主要职责
中国科学院贯彻落实党中央关于科技创新的方针政策和决策部署,在履行职责过程中坚持党中央对科技工作的集中统一领导。主要职责是:
一、开展使命导向的自然科学领域基础研究,承担国家重大基础研究、应用基础研究、前沿交叉共性技术研究和引领性颠覆性技术研究任务,打造原始创新策源地。 更多+
院况简介
中国科学院是国家科学技术界最高学术机构、国家科学技术思想库,自然科学基础研究与高技术综合研究的国家战略科技力量。
1949年,伴随着新中国的诞生,中国科学院成立。建院70余年来,中国科学院时刻牢记使命,与科学共进,与祖国同行,以国家富强、人民幸福为己任,人才辈出,硕果累累,为我国科技进步、经济社会发展和国家安全作出了不可替代的重要贡献。 更多+
院领导集体
科技奖励
科技期刊
科技专项
科研进展/ 更多
工作动态/ 更多
工作动态/ 更多
中国科学院学部
中国科学院院部

语音播报

11月27日,中国科学院上海营养与健康研究所章海兵研究组等在Advanced Science上,在线发表了题为ABIN1 (Q478) is required to prevent hematopoietic deficiencies through regulating type I IFNs expression的研究论文。研究发现,泛素结合蛋白ABIN1通过泛素结合功能域调控I-型干扰素的产生,在类骨髓增生异常综合症(MDS-liked diseases)的发生发展中起到关键作用,为骨髓增生异常综合症(MDSs)的治疗提供了新的思路和策略。
ABIN1(A20-binding inhibitor of NF-κB activation)是泛素结合蛋白,可以通过识别多聚泛素链将泛素调节蛋白招募至目的蛋白,对细胞死亡和天然免疫调控颇为重要。TNIP1基因编码ABIN1蛋白,位于人类第五条染色体的长臂端,而这一区域是5q缺失类型骨髓增生异常综合症病人中高频率发生缺失的染色体区域。此外,科学家在小鼠模型研究中发现TNIP1基因的缺失对小鼠造血系统发育至关重要,而ABIN1蛋白是否参与骨髓造血异常增生综合症(MDS)发生发展尚不清楚。
该研究构建了ABIN1泛素结合功能域关键位点失活突变小鼠(Abin1Q478H/Q478H),并通过对该小鼠造血系统的分析,发现Abin1Q478H/Q478H小鼠外周血中红细胞和血小板数量减少、骨髓中出现异常小巨核细胞以及髓外代偿性造血的发生。这表明Abin1Q478H/Q478H小鼠患有类骨髓增生异常综合症的疾病(MDS-liked diseases),并呈现年龄相关性进展。科研人员基于前期研究发现,ABIN1参与细胞死亡的调控作用,并通过遗传学的方式,将细胞程序性坏死关键基因突变或者缺失小鼠(Ripk1K45A/K45A、Ripk3-/-、Mlkl-/-)与Abin1Q478H/Q478H小鼠进行杂交并得到纯合小鼠。研究显示,仅敲除Ripk3可以缓解Abin1Q478H/Q478H小鼠的贫血和髓外代偿性造血现象,但Ripk1K45A/K45A点突变和Mlkl基因敲除没有类似于Ripk3敲除小鼠的明显缓解效果,表明Abin1Q478H/Q478H小鼠的类骨髓增生异常综合症的发生依赖于RIPK3的非细胞程序性坏死功能。
进一步的机制研究表明,I-型干扰素及ISGs基因的mRNA水平在小鼠的骨髓来源的巨噬细胞和骨髓干祖细胞中的表达显著上升,这提示I-型干扰素的过度产生可能是Abin1Q478H/Q478H小鼠类骨髓增生异常综合症的形成原因。研究还发现,ABIN1(Q478H)突变蛋白导致TRAF3的泛素化增加,进而影响下游I-型干扰素的产生。该研究进一步构建了Abin1Q478H/Q478H Ifnar1-/-小鼠。科研人员通过对该小鼠的系统分析发现,缺失I-型干扰素受体(Ifnar1)后,Abin1Q478H/Q478H小鼠的外周血中红细胞和血小板的数量显著增加、血红蛋白浓度显著提高、血小板平均体积大小显著降低,以及髓外代偿造血和骨髓衰竭程度均有显著恢复。上述成果表明,Abin1Q478H/Q478H小鼠的造血缺陷依赖于IFNAR1受体介导的I-型干扰素信号通路。该研究揭示了泛素结合蛋白ABIN1影响I-型干扰素表达,进而调控骨髓增生异常综合症的新机制,为治疗骨髓增生异常综合症提供了新的靶点和思路。
该研究由营养与健康所和上海交通大学医学院附属第九人民医院合作完成。研究工作得到国家重点研发计划、国家自然科学基金、上海市“科技创新行动计划”等的资助,并获得营养与健康所所级公共技术中心分析测试技术平台和实验动物技术平台等的支持。
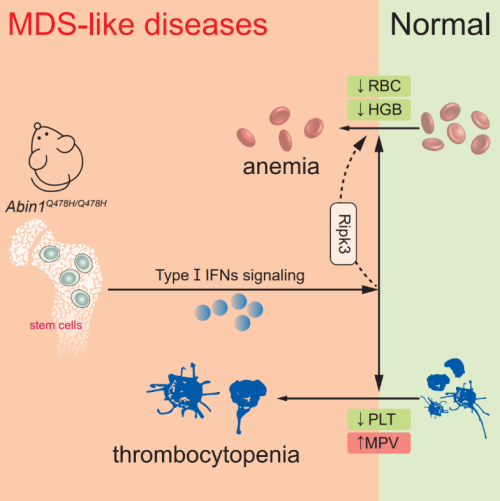
ABIN1泛素结合功能介导I-型干扰素表达控骨髓增生异常综合症

© 1996 - 中国科学院 版权所有 京ICP备05002857号-1  京公网安备110402500047号 网站标识码bm48000002
京公网安备110402500047号 网站标识码bm48000002
地址:北京市西城区三里河路52号 邮编:100864
电话: 86 10 68597114(总机) 86 10 68597289(总值班室)














