主要职责
中国科学院贯彻落实党中央关于科技创新的方针政策和决策部署,在履行职责过程中坚持党中央对科技工作的集中统一领导。主要职责是:
一、开展使命导向的自然科学领域基础研究,承担国家重大基础研究、应用基础研究、前沿交叉共性技术研究和引领性颠覆性技术研究任务,打造原始创新策源地。 更多+
院况简介
中国科学院是国家科学技术界最高学术机构、国家科学技术思想库,自然科学基础研究与高技术综合研究的国家战略科技力量。
1949年,伴随着新中国的诞生,中国科学院成立。建院70余年来,中国科学院时刻牢记使命,与科学共进,与祖国同行,以国家富强、人民幸福为己任,人才辈出,硕果累累,为我国科技进步、经济社会发展和国家安全作出了不可替代的重要贡献。 更多+
院领导集体
科技奖励
科技期刊
科技专项
科研进展/ 更多
工作动态/ 更多
工作动态/ 更多
中国科学院学部
中国科学院院部

语音播报

近日,中国科学院国家纳米科学中心研究员陈春英团队在细胞内吞过程中“纳米蛋白冠”的演化模式及其对细胞内蛋白稳态和能量代谢的扰动研究方面取得重要进展。相关研究成果以Dynamic intracellular exchange of nanomaterials’ protein corona perturbs proteostasis and remodels cell metabolism为题,发表在《美国国家科学院院刊》(PNAS)上。
当纳米颗粒进入生物体系时,生物流体的生物分子迅速与纳米颗粒表面结合,其中与血液中蛋白质分子互作形成的“纳米蛋白冠”作为起始步骤,对纳米颗粒体内的输运和命运影响巨大,引起科学界关注。“纳米蛋白冠”的形成如何影响纳米颗粒在不同屏障系统组织和细胞的识别、转运、分布、功能和生物效应,是纳米材料生物医学应用的“黑匣子”问题,制约纳米药物的递送效率,并影响其有效性和安全性。
该领域研究的重要挑战之一是“纳米蛋白冠”的复杂性,而该复杂性受不同组织器官中生物分子的多样性及生理病理状态的影响。目前,关于蛋白冠的蛋白组成和结构特性如何随纳米颗粒所处的生物微环境不同而发生变化,存在认知不明、机理不清的问题。
科研团队利用创新应用多维度多组学(蛋白组学、代谢组学、脂质组学)、分子间互作以及原位质谱成像等分析技术,首次揭示了“纳米蛋白冠”的蛋白组成在细胞转运过程中的动态演化模式。研究以纳米金颗粒为模式纳米颗粒,探究了蛋白冠从血液系统到细胞内的动态演化过程(血液-溶酶体-细胞质),当纳米颗粒由血液环境经过细胞内吞进入溶酶体,再从溶酶体逃逸进入细胞质后,其表面的蛋白组成发生巨大变化,大多被细胞内蛋白质分子所替代,只保留部分血液环境中形成的蛋白冠成分。纳米蛋白冠的胞内演化会扰乱细胞内的蛋白稳态(proteostasis),引发伴侣蛋白(HSC70、HSP90等)和丙酮酸激酶M2(PKM2)在胞内纳米蛋白冠表面的富集,激发伴侣蛋白介导的自噬反应(Chaperone mediated autophagy,CMA);进一步影响细胞糖酵解,引起细胞能量代谢的改变,调控细胞脂质代谢过程。该研究阐明了纳米颗粒从血液到亚细胞微环境转运过程中的演化模式,发现了“纳米蛋白冠”的胞内微环境特异性,进而重塑细胞代谢,为剖析纳米-生物界面调控纳米材料复杂生物学效应提供了新认识和理论支撑。
研究工作得到国家重点研发计划、国家自然科学基金创新研究群体项目、中科院战略性先导科技专项(B类)等的支持。
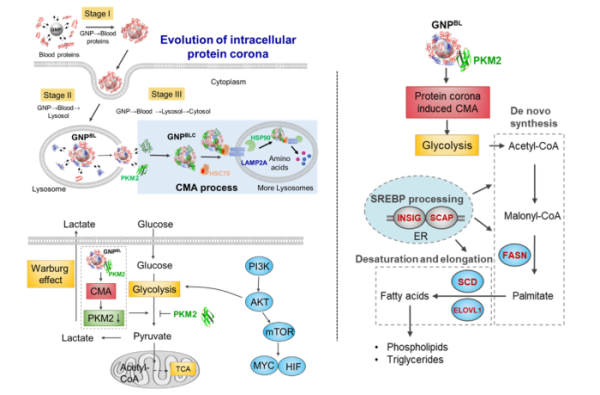
纳米蛋白冠在细胞内吞转运过程中的演化模式示意图:从血液-溶酶体-细胞质的转运过程中,蛋白冠的组分与胞内蛋白(伴侣蛋白、代谢激酶)的交换引发伴侣蛋白介导的自噬活性的升高,并选择性地重塑细胞代谢。
扫一扫在手机打开当前页

© 1996 - 中国科学院 版权所有 京ICP备05002857号-1  京公网安备110402500047号 网站标识码bm48000002
京公网安备110402500047号 网站标识码bm48000002
地址:北京市西城区三里河路52号 邮编:100864
电话: 86 10 68597114(总机) 86 10 68597289(总值班室)














