主要职责
中国科学院贯彻落实党中央关于科技创新的方针政策和决策部署,在履行职责过程中坚持党中央对科技工作的集中统一领导。主要职责是:
一、开展使命导向的自然科学领域基础研究,承担国家重大基础研究、应用基础研究、前沿交叉共性技术研究和引领性颠覆性技术研究任务,打造原始创新策源地。 更多+
院况简介
中国科学院是国家科学技术界最高学术机构、国家科学技术思想库,自然科学基础研究与高技术综合研究的国家战略科技力量。
1949年,伴随着新中国的诞生,中国科学院成立。建院70余年来,中国科学院时刻牢记使命,与科学共进,与祖国同行,以国家富强、人民幸福为己任,人才辈出,硕果累累,为我国科技进步、经济社会发展和国家安全作出了不可替代的重要贡献。 更多+
院领导集体
科技奖励
科技期刊
科技专项
科研进展/ 更多
工作动态/ 更多
工作动态/ 更多
中国科学院学部
中国科学院院部

语音播报

近日,中国科学院院士、中科院生物物理研究所/中科院纳米酶工程实验室研究员阎锡蕴团队在Nano Today上,在线发表关于铁蛋白药物载体(Ferritin Drug Carrier)药物装载方法的最新研究成果,该研究揭示铁蛋白药物载体表面存在药物通道,为铁蛋白药物临床转化奠定了理论基础。
铁蛋白是天然存在于人体细胞中的储铁蛋白,在人体内的铁平衡和细胞抗氧化中具有关键作用。铁蛋白具有独特的壳核结构,外壳直径12nm,由24 个蛋白亚基自组装形成;内腔直径8nm,可以装载治疗药物。在前期工作中,研究发现人重链铁蛋白识别肿瘤标志分子转铁蛋白受体(TfR1)(Nature Nanotechnology, 2012),进而赋予铁蛋白新型药物载体功能(PNAS, 2014),并提出铁蛋白药物载体(Ferritin drug carrier, FDC)新概念(Journal of Controlled Release, 2019)。FDC类似于抗体偶联药物(ADC),通过其对受体的特异识别功能将负载的小分子药物靶向运输到肿瘤组织;与ADC相比,具有药物装载能力、热稳定性和易生产性等属性上的优势。然而,有关FDC的载药机理尚不明确。
阎锡蕴团队通过铁蛋白晶体结构分析,开展突变体设计与载药的相关性研究,发现药物进入铁蛋白内腔是通过特定的通道。该通道由第89-92位及其附近的氨基酸残基组成的,位于铁蛋白表面二重对称轴处的柔性区域。该药物装载通道的“开关”受温度调控(如图)。环境温度的提升有助于89-92位氨基酸残基摆动到远离二重轴的位置,通道“打开”,药物从此处进入铁蛋白内腔。研究基于这一发现,通过温度调节将阿霉素药物装载到铁蛋白内腔。动物实验结果表明该铁蛋白药物的稳定性高、安全性好、抗肿瘤效果优异。该药物通道对于小分子药物具有普适性,利用该通道也可以装载顺铂、奥沙利铂、表阿霉素等其他小分子药物,具有发展成为新药技术平台的潜质。
阎锡蕴和研究员范克龙为论文的共同通讯作者,郑州大学基础医学院博士江冰和生物物理所博士陈雪晖为论文的共同第一作者。研究工作得到国家自然科学基金、中科院战略性先导科技专项等的资助。上海同步辐射光源(SSRF)为该研究提供技术支持。
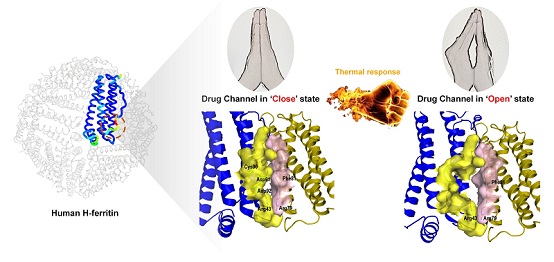
铁蛋白药物装载通道的“开-关”受温度调控
扫一扫在手机打开当前页

© 1996 - 中国科学院 版权所有 京ICP备05002857号-1  京公网安备110402500047号 网站标识码bm48000002
京公网安备110402500047号 网站标识码bm48000002
地址:北京市西城区三里河路52号 邮编:100864
电话: 86 10 68597114(总机) 86 10 68597289(总值班室)














