|
|
|||||||
| 营养与健康所发现乙醛脱氢酶2调控肝脏胆固醇代谢机制 |
| 文章来源: | 上海营养与健康研究所 | 发布时间: | 2021-03-11 |
|
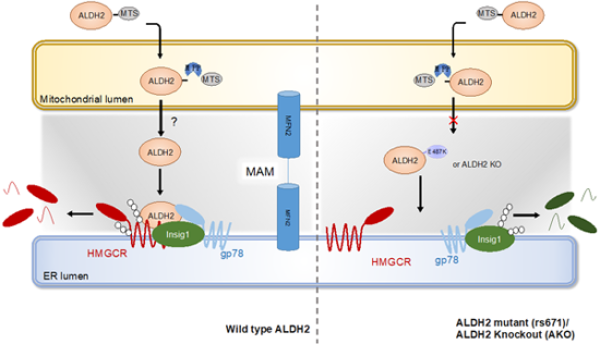
3月10日,Redox Biology在线发表了中国科学院上海营养与健康研究所尹慧勇课题组题为Acetaldehyde Dehydrogenase 2 Regulates HMG-CoA Reductase Stability and Cholesterol Synthesis in the Liver的最新研究成果。该研究揭示了乙醛脱氢酶2(Acetaldehyde Dehydrogenase 2,ALDH2)通过调控肝脏胆固醇从头合成过程中一个关键决速酶,3-羟基-3-甲基戊二酸单酰辅酶A还原酶(3-hydroxy-3-methyl glutaryl coenzyme A reductase,HMGCR)的蛋白稳定性来影响胆固醇代谢新机制。 心血管疾病发生率和死亡率较高,动脉粥样硬化是造成心血管疾病发生发展的主要原因之一。血清中的高胆固醇水平是心血管疾病发生的独立风险因素,降低胆固醇是预防和治疗动脉粥样硬化和心血管疾病的主要手段。现今,临床上降胆固醇一线药物他汀是靶向HMGCR从而抑制胆固醇合成。 乙醛脱氢酶2(ALDH2)主要负责催化将饮酒产生的乙醛氧化成乙酸,以及代谢氧化应激脂质过氧化产生的活性醛类等。在动脉粥样硬化过程中,脂质过氧化与炎症反应是两个重要的风险因素。人体中有一个核苷酸多态性位点(SNP,rs671),携带这个突变的人群由于ALDH2酶活降低表现为饮酒后脸红。该突变影响全球8%的人群,而亚洲人群中有30-50%的人携带该突变。人群研究的数据显示这些人群除了喝酒脸红外,心血管疾病的风险也显著增加,相关分子机制有待进一步明确。试验室前期研究发现,ALHD2与低密度脂蛋白受体LDLR以及AMPK相互作用,影响泡沫巨噬细胞的形成(J Clin Invest, 2019),首次阐明了一个ALDH2突变增加动脉粥样硬化风险的独立于饮酒之外的分子机制。另外,既往的人群数据也显示ALDH2突变与胆固醇代谢相关,但分子机制不明。 研究中,科研人员在ALDH2基因敲除及rs671敲入小鼠中观察到即使喂养普通食物也引起肝脏和血清中总胆固醇和低密度脂蛋白水平的升高。利用代谢组学和代谢流分析发现ALDH2基因敲除小鼠胆固醇合成增加;小鼠胆固醇水平的升高可被他汀类药物抑制,提示ALDH2可能参与调控胆固醇合成酶HMGCR。在细胞实验中,研究发现ALDH2直接影响HMGCR的泛素化降解:ALDH2促进HMGCR与Insig1/SCAP/gp78的相互作用,抑制胆固醇合成,这种作用在ALDH2突变体中显著减弱。进一步的机制研究显示,在胆固醇升高时,线粒体的ALDH2通过线粒体与内质网接触的膜结构(Mitochondria-Associated membrane with ER,MAM)转移至内质网,促进HMGCR的泛素化降解。在ALDH2基因敲除或rs671敲入模型中,HMGCR的蛋白稳定性增加从而促进胆固醇合成(如图所示)。该研究发现了胆固醇代谢调控的新机制,并提示在ALDH2突变人群心血管疾病的风险增加或与胆固醇代谢失调有关;临床降胆固醇药物他汀可以有效抑制胆固醇水平的升高。 营养与健康所研究员尹慧勇为论文通讯作者,博士研究生仲珊珊、李露晓为论文共同第一作者。研究工作受到复旦大学教授孙爱军和任骏、武汉大学教授宋保亮、中科院分子细胞科学卓越创新中心研究员李伯良、加拿大艾伯塔大学教授章大卫、美国佐治亚州立大学教授邹明辉等的帮助,得到国家自然科学基金委员会、科学技术部和中科院的资助,并获得营养与健康所公共技术平台和动物平台的支持。
乙醛脱氢酶2调控肝脏胆固醇代谢机制示意图 |
| © 1996 - 中国科学院 版权所有 备案序号:京ICP备05002857号 联系我们 地址:北京市三里河路52号 邮编:100864 |