主要职责
中国科学院贯彻落实党中央关于科技创新的方针政策和决策部署,在履行职责过程中坚持党中央对科技工作的集中统一领导。主要职责是:
一、开展使命导向的自然科学领域基础研究,承担国家重大基础研究、应用基础研究、前沿交叉共性技术研究和引领性颠覆性技术研究任务,打造原始创新策源地。 更多+
院况简介
中国科学院是国家科学技术界最高学术机构、国家科学技术思想库,自然科学基础研究与高技术综合研究的国家战略科技力量。
1949年,伴随着新中国的诞生,中国科学院成立。建院70余年来,中国科学院时刻牢记使命,与科学共进,与祖国同行,以国家富强、人民幸福为己任,人才辈出,硕果累累,为我国科技进步、经济社会发展和国家安全作出了不可替代的重要贡献。 更多+
院领导集体
科技奖励
科技期刊
科技专项
科研进展/ 更多
工作动态/ 更多
工作动态/ 更多
中国科学院学部
中国科学院院部

语音播报

近日,Molecular Metabolism在线发表了中国科学院上海营养与健康研究所陈雁研究组题为PAQR9 regulates hepatic ketogenesis and fatty acid oxidation during fasting by modulating protein stability of PPARα的研究论文。 该研究首次发现内质网蛋白PAQR9能通过调节肝脏细胞的转录因子PPARα的稳定性,参与饥饿诱导肝脏酮体生成和脂肪酸氧化。
饥饿和进食的交替是生命根本的生理过程,其中可发生大量代谢状态变化。肝脏是体内重要的代谢器官,在饥饿的过程中会响应营养缺乏信号,进行脂肪酸氧化和酮体生成,为机体提供能量。该过程会受转录因子调控,其中PPARα是核心转录因子,PPARα基因缺失会导致饥饿过程中脂肪酸氧化降低。研究组前期研究已发现,PPARα会通过E3泛素连接酶HUWE1的泛素化修饰介导蛋白酶体途径降解。
近期,研究组博士研究生林毅君等通过大数据分析和动物实验发现,在饥饿状态下的肝脏中,PAQR9是下调最显著的基因之一,并鉴定出饥饿-进食过程中PAQR9的表达受到PPARγ的直接调控。通过对PAQR9基因敲除小鼠进行一系列代谢表征研究,发现敲除PAQR9不影响小鼠正常进食情况下的代谢状态,但会显著降低小鼠饥饿情况下肝脏的酮体生成和脂肪酸氧化能力。分子机制研究发现,敲除小鼠肝脏中的PPARα,转录水平不会受到影响,但蛋白含量显著下降。细胞实验证实,PAQR9能够降低PPARα泛素化导致的降解。进一步研究PAQR9对PPARα泛素化水平的调控机制,发现PAQR9能够和介导PPARα降解的HUWE1竞争性结合以保护PPARα不被降解。体外HUWE1敲除和体内PPARα激动剂回补实验均充分验证了PAQR9竞争性结合HUWE1保护PPARα蛋白稳定性模型的可靠性。综上所述,该研究揭示出内质网蛋白PAQR9能够通过泛素化调控转录因子PPARα的活性,揭示出一个新的肝脏脂代谢调控机制。
研究工作得到国家自然科学基金委和科技部的资助,以及营养与健康所公共技术平台和动物平台的支持。
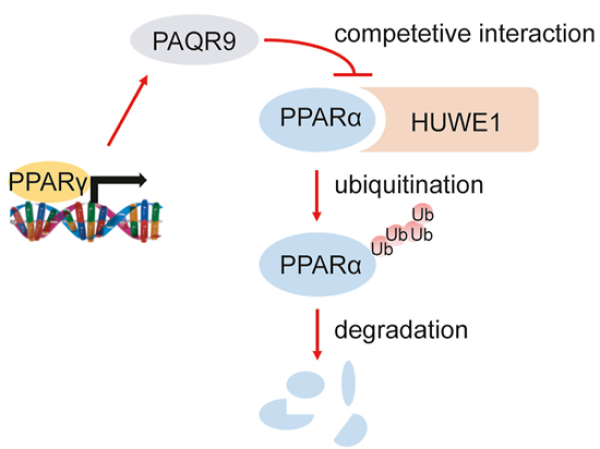
PAQR9竞争性结合HUWE1以保护PPARα蛋白稳定性
扫一扫在手机打开当前页

© 1996 - 中国科学院 版权所有 京ICP备05002857号-1  京公网安备110402500047号 网站标识码bm48000002
京公网安备110402500047号 网站标识码bm48000002
地址:北京市西城区三里河路52号 邮编:100864
电话: 86 10 68597114(总机) 86 10 68597289(总值班室)














