主要职责
中国科学院贯彻落实党中央关于科技创新的方针政策和决策部署,在履行职责过程中坚持党中央对科技工作的集中统一领导。主要职责是:
一、开展使命导向的自然科学领域基础研究,承担国家重大基础研究、应用基础研究、前沿交叉共性技术研究和引领性颠覆性技术研究任务,打造原始创新策源地。 更多+
院况简介
中国科学院是国家科学技术界最高学术机构、国家科学技术思想库,自然科学基础研究与高技术综合研究的国家战略科技力量。
1949年,伴随着新中国的诞生,中国科学院成立。建院70余年来,中国科学院时刻牢记使命,与科学共进,与祖国同行,以国家富强、人民幸福为己任,人才辈出,硕果累累,为我国科技进步、经济社会发展和国家安全作出了不可替代的重要贡献。 更多+
院领导集体
科技奖励
科技期刊
科技专项
科研进展/ 更多
工作动态/ 更多
工作动态/ 更多
中国科学院学部
中国科学院院部

语音播报

3月4日,中国科学院生物物理研究所孙飞课题组与德国马克斯-普朗克研究所Hartmut Michel课题组,在《德国应用化学》上发表了题为The unusual homodimer of a heme-copper terminal oxidase allows itself to utilize two electron donors的研究论文。该工作研究了一种来自超嗜热菌的特殊的血红素-铜终端氧化酶,通过解析其高分辨率冷冻电镜结构,发现了其既能氧化细胞色素c又能氧化氢醌的独特催化机制,并发现了它的质子通道和氧气通道具有新颖的结构特征。这些结果进一步丰富了人类对于不同物种间细胞色素c氧化酶结构差异的理解,揭示了细胞色素c氧化酶在极端环境下的进化适应性。
血红素-铜终端氧化酶家族蛋白是一类重要金属蛋白酶,负责高效催化电子从细胞色素c或氢醌传递给氧分子,将氧气还原为水。该家族成员是多亚基复合物,在哺乳动物线粒体中由14个亚基组成,而在大多数细菌中由3个亚基组成。它们的核心催化亚基I非常保守,结合有两个血红素和一个铜原子,其中铜原子与高自旋血红素的铁原子形成双核中心;亚基II通常结合有两个铜原子,形成双核中心。细胞色素c氧化酶属于血红素-铜终端氧化酶家族成员,之前研究显示,它一般只能使用细胞色素c作为电子供体。不同物种间的细胞色素c氧化酶结构上存在显著差异,包括亚基数目、亚基I/II的跨膜螺旋数、质子通道及氧气通道结构特征等,探究这些细胞色素c氧化酶的不同结构,可揭示该蛋白的进化趋势和发挥不同生物学功能的结构基础。
Aquifex aeolicus是细菌最古老的分支、最嗜热的菌之一,最适生长温度85-95℃,分布在世界各地的高温液体环境中,包括陆地和海洋,能适应多种极端环境。2012年,Hartmut Michel课题组首次报道了该嗜热菌有一种独特的细胞色素c氧化酶,既能氧化细胞色素c又能氧化氢醌,但催化机制和进化上的意义仍未知。孙飞课题组与Hartmut Michel课题组经过多年合作,近期利用冷冻电镜单颗粒技术解析了A. aeolicus细胞色素c氧化酶的三维结构,分辨率达到了3.4埃。它形成一个独特的同源二聚体,结合形式不同于以往报道的其它物种的细胞色素c氧化酶。在它的二聚体界面处,有两个底物氢醌分子(NQ)紧密结合在复合体上,形成一条潜在的电子传递链,使得整个细胞色素c氧化酶在氧化细胞色素c的同时又能氧化氢醌。研究表明这种独特的二聚化特征对于双底物催化是必要的。结构分析证实,A. aeolicus细胞色素c氧化酶为了适应低氧、高温环境,它的质子通道效率显著降低,而氧气通道效率增加。此外,与A. aeolicus呼吸链复合物III类似,它也有一些独特的热稳定性结构特征。这些研究成果进一步丰富了人类对细胞色素c氧化酶的结构和功能的认识。这也是研究团队继解析A. aeolicus呼吸链复合物III结构的又一重要进展,有利于深入了解这一古老超嗜热菌的呼吸作用以及呼吸链复合物为适应极端条件采取的进化策略。
生物物理所研究员孙飞、副研究员朱赟,德国马普所教授Hartmut Michel与博士彭国宏、曾辉为论文的共同通讯作者,孙飞课题组博士研究生朱国梁、已毕业硕士研究生张双博,以及曾辉为论文的共同第一作者。研究得到国家自然科学基金、国家重点研发计划、中科院战略性先导科技专项等的资助。数据收集等工作得到生物物理所生物成像中心(正高级工程师黄小俊、工程师朱博玲、工程师李许静等)的支持。
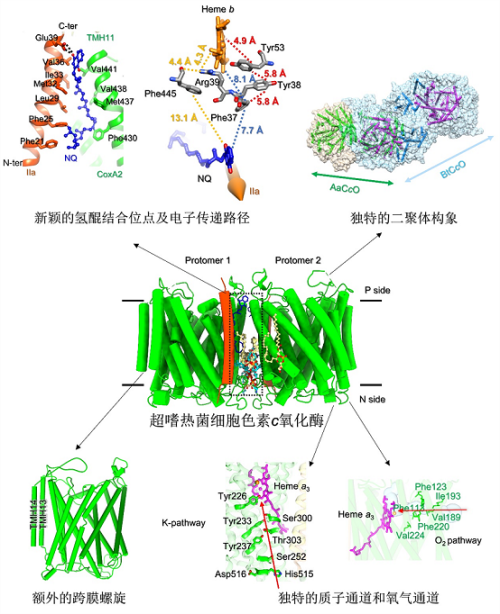
超嗜热菌细胞色素c氧化酶冷冻电镜三维结构。独特的二聚体构象允许其既能氧化细胞色素c又能氧化氢醌,额外的跨膜螺旋、质子通道和氧气通道等新颖结构特征揭示了细胞色素c氧化酶在极端环境下的进化适应性
扫一扫在手机打开当前页

© 1996 - 中国科学院 版权所有 京ICP备05002857号-1  京公网安备110402500047号 网站标识码bm48000002
京公网安备110402500047号 网站标识码bm48000002
地址:北京市西城区三里河路52号 邮编:100864
电话: 86 10 68597114(总机) 86 10 68597289(总值班室)














