主要职责
中国科学院贯彻落实党中央关于科技创新的方针政策和决策部署,在履行职责过程中坚持党中央对科技工作的集中统一领导。主要职责是:
一、开展使命导向的自然科学领域基础研究,承担国家重大基础研究、应用基础研究、前沿交叉共性技术研究和引领性颠覆性技术研究任务,打造原始创新策源地。 更多+
院况简介
中国科学院是国家科学技术界最高学术机构、国家科学技术思想库,自然科学基础研究与高技术综合研究的国家战略科技力量。
1949年,伴随着新中国的诞生,中国科学院成立。建院70余年来,中国科学院时刻牢记使命,与科学共进,与祖国同行,以国家富强、人民幸福为己任,人才辈出,硕果累累,为我国科技进步、经济社会发展和国家安全作出了不可替代的重要贡献。 更多+
院领导集体
科技奖励
科技期刊
科技专项
科研进展/ 更多
工作动态/ 更多
工作动态/ 更多
中国科学院学部
中国科学院院部

语音播报

人类基因组包含大约31.6亿个DNA碱基对,线性DNA分子作为庞大遗传信息的载体一般都比较长(人类一条染色体的DNA长度约为2米),生命通过组蛋白将DNA分子有序组织压缩形成微米级别的染色质存储到细胞核中。核小体是染色质的结构和功能的最基本单元,其中DNA缠绕在组蛋白巴聚体周围约两圈,完成对DNA的第一次组装压缩。为了读取基因密码,染色质中的DNA需要时刻从组蛋白八聚体上解离,信息读取完毕后DNA快速正确地结合组蛋白八聚体恢复染色质结构。因此染色质结构高度动态的开合是细胞核内染色质的主旋律。为了保证精确的读取基因密码,动态调控染色质结构,生命进化出了纷繁复杂的调控方式,比如DNA甲基化修饰,组蛋白甲基化、乙酰化、泛素化等修饰,组蛋白变体,各种染色质伴侣,多种染色质重塑因子。如何定量地描述这些调控因素对染色质的影响,是人们正确认识基因转录机理的关键所在。单分子力谱技术是精确操控生物大分子,在单分子水平上跟踪生物大分子动态结构和化学反应的利器,帮助人们以全新的视角定量解析生物大分子的动态结构,回答以上关键问题。
中国科学院物理研究所/北京凝聚态物理国家研究中心软物质实验室SM1组副研究员李伟长期从事单分子力谱技术的发展和应用,与生物学家合作在染色质动态结构和调控方面取得一系列进展(Molecular Cell 2016,2018)。最近,与首都医科大学教授陈萍课题组以及中科院生物物理研究所研究员李国红课题组合作,在国际上首次测量了组蛋白H2AK119泛素修饰对核小体结构的影响,并且建立了单分子系统实时观察去泛素酶USP21敲去泛素的逆过程。利用刚刚建立的基于GPU计算的高通量高分辨单分子磁镊力谱技术,解析了组蛋白H2AK119位置的单泛素修饰能够锁定DNA剥离,将核小体自由能从30kJ/mol降低至200kJ/mol,极大增强了核小体结构的稳定性。并且,进一步确定出一个H2AK119泛素修饰负责锁定半圈核小体DNA。这部分工作直接回答了H2AK119泛素修饰在基因沉默方面发挥作用的分子机理。最后,他们实时再现了去泛素酶USP21结合核小体上,敲去H2AK119泛素的动态过程,进一步证明了组蛋白H2A泛素修饰通过锁定DNA,阻止DNA从组蛋白八聚体上剥离,完成基因沉默的功能。相关工作发表在2020年JACS期刊,并被推荐为Top5%文章。
李伟和陈萍为文章的共同通讯作者,物理所博士研究生肖雪、生物物理所助理研究员刘翠芳及硕士研究生裴迎新为共同第一作者。该工作得到国家自然科学基金委、科技部和中科院前沿重点项目的资助。
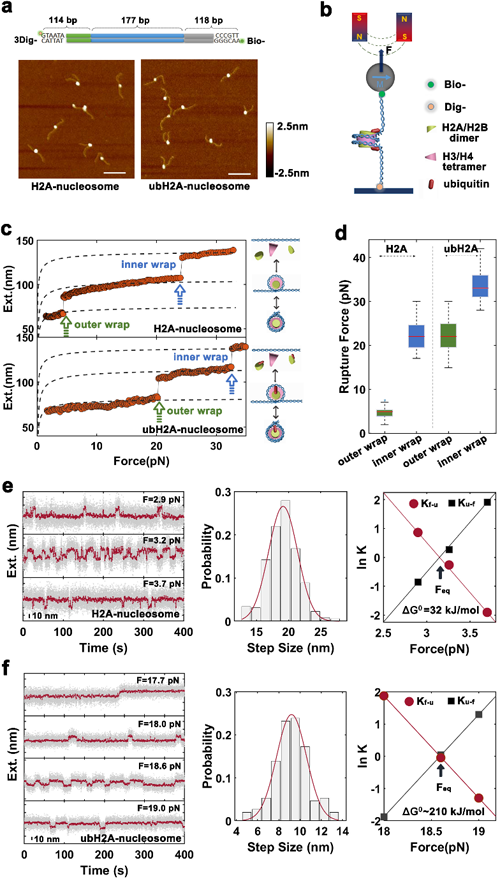
图1. 单分子力谱技术解析H2A泛素增强核小体力学稳定性。(a)核小体AFM图像。(b)磁镊示意图。(c)常规核小体(上)和泛素核小体的拆解动力学。(d)拆解外力统计。(e)常规核小体折叠去折叠动态结构恒力跟踪。(f)泛素核小体折叠去折叠动态结构恒力跟踪。
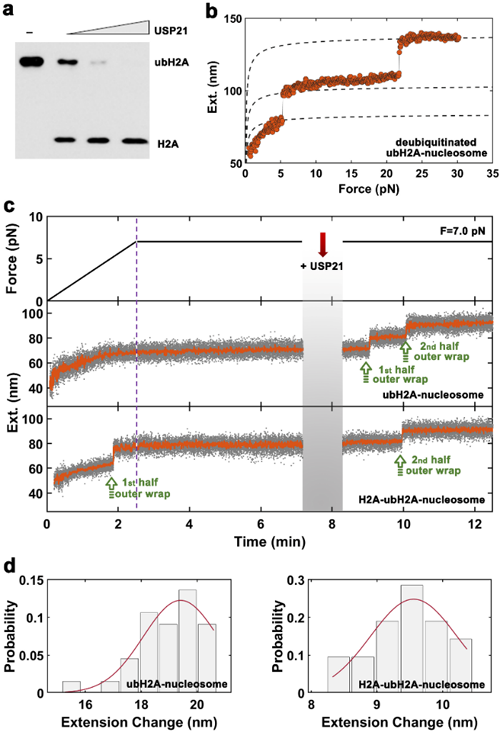
图2.去泛素酶USP21结合核小体动力学过程。(a)USP21结合组蛋白H2A胶图。(b)USP21处理后的核小体回归常规核小体状态。(c)USP21结合双泛素(上)和单泛素核小体(下)动力学过程。
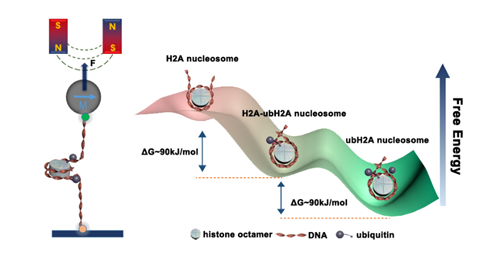
图3.泛素修饰增强核小体力学稳定性,实现基因沉默的调控功能。

© 1996 - 中国科学院 版权所有 京ICP备05002857号-1  京公网安备110402500047号 网站标识码bm48000002
京公网安备110402500047号 网站标识码bm48000002
地址:北京市西城区三里河路52号 邮编:100864
电话: 86 10 68597114(总机) 86 10 68597289(总值班室)














