主要职责
中国科学院贯彻落实党中央关于科技创新的方针政策和决策部署,在履行职责过程中坚持党中央对科技工作的集中统一领导。主要职责是:
一、开展使命导向的自然科学领域基础研究,承担国家重大基础研究、应用基础研究、前沿交叉共性技术研究和引领性颠覆性技术研究任务,打造原始创新策源地。 更多+
院况简介
中国科学院是国家科学技术界最高学术机构、国家科学技术思想库,自然科学基础研究与高技术综合研究的国家战略科技力量。
1949年,伴随着新中国的诞生,中国科学院成立。建院70余年来,中国科学院时刻牢记使命,与科学共进,与祖国同行,以国家富强、人民幸福为己任,人才辈出,硕果累累,为我国科技进步、经济社会发展和国家安全作出了不可替代的重要贡献。 更多+
院领导集体
科技奖励
科技期刊
科技专项
科研进展/ 更多
工作动态/ 更多
工作动态/ 更多
中国科学院学部
中国科学院院部

语音播报

1月17日,中国科学院上海营养与健康研究所时玉舫/王莹团队在《美国国家科学院院刊》(PNAS)在线发表了题为Scd1 controls de novo beige fat biogenesis through succinate-dependent regulation of mitochondrial complex II 的研究论文。博士研究生刘轲莉以硬脂酰辅酶A去饱和酶1(Stearoyl-CoA desaturase 1, Scd1)为研究切入点,首次揭示了Scd1与琥珀酸之间的调控关系,及其决定脂肪前体细胞向米色脂肪细胞分化的调控机制,为预防和治疗肥胖及相关代谢紊乱性疾病提供了新的策略。
米色脂肪细胞,一种能够消耗脂肪进行呼吸产热的“好”脂肪,被认为是抵抗肥胖的有效治疗方式而备受关注。研究表明,米色脂肪可以由白色脂肪转化形成,也能通过二者共同的前体细胞(adipose tissue derived mesenchymal stem cells, ADSCs)分化形成。事实上,诸如低温、运动和斋戒等诱导米色脂肪细胞产生的方式,是机体通过一系列复杂机制协调二者来实现的。除了这些传统方式,如何特异性地靶向米色脂肪细胞的产生仍然是该领域研究的重点问题。
Scd1作为单不饱和脂肪酸合成的限速酶,是脂肪酸合成所必需的,为机体生命活动提供基础保障的同时,也参与调节不同器官的代谢活动。时玉舫/王莹团队利用Scd1基因突变小鼠、基因敲除小鼠和条件性敲除小鼠,揭示了Scd1缺失对于米色脂肪细胞的促进作用并非依赖于白色脂肪细胞的米色化,而是直接调控ADSCs向米色脂肪细胞的分化过程。ADSCs中特异敲除Scd1的小鼠明显抵抗肥胖及其相关胰岛素抵抗的发生和进展。Scd1的缺失促进琥珀酸的累积进而上调线粒体复合物Ⅱ活性,最终决定脂肪前体细胞向米色脂肪细胞分化的倾向性。该团队发现以琥珀酸单独处理脂肪前体细胞便可以促进其向米色脂肪细胞的分化。更重要的是,给予小鼠饮用富含琥珀酸的水可促使脂肪组织中米色脂肪的大量产生,使小鼠有效抵抗高脂饮食诱导的肥胖发生。此项研究证明了Scd1与琥珀酸之间的负向调控关系对脂肪前体细胞向白色和米色脂肪细胞分化的决定作用,揭示了琥珀酸治疗肥胖及其相关代谢紊乱性疾病的潜能,为临床治疗代谢性疾病提供了新思路。
刘轲莉为该研究的第一作者,时玉舫与王莹为共同通讯作者。该研究是中科院营养与健康所、上海科技大学、苏州大学附属第一医院和罗马第二大学的合作研究,得到了营养与健康所研究员孔祥银和上海交通大学教授李保界的支持以及苏州大学附属第一医院教授邵常顺的指导。经费支持来自于国家科技部重点研发计划、中科院战略性先导专项、国家自然科学基金委、基金委中意国际合作项目、中科院青年创新促进会等,同时研究得到营养与健康所公共技术平台和动物平台的支持和帮助。
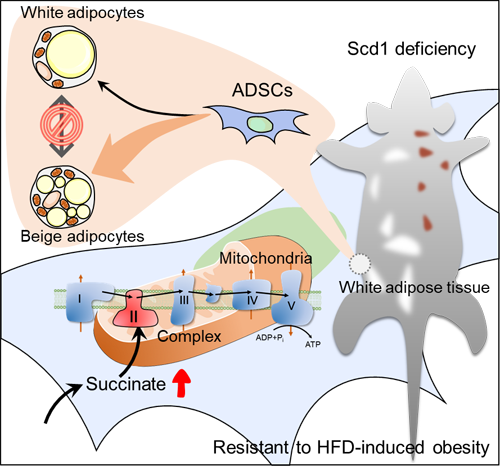
图注:Scd1缺失导致脂肪前体细胞(ADSCs)内琥珀酸含量升高,进而促进线粒体复合物2活性,使得ADSCs更倾向于米色脂肪细胞分化,以此导致小鼠体内米色脂肪大量累积并抵抗高脂饮食诱导的肥胖发生。

© 1996 - 中国科学院 版权所有 京ICP备05002857号-1  京公网安备110402500047号 网站标识码bm48000002
京公网安备110402500047号 网站标识码bm48000002
地址:北京市西城区三里河路52号 邮编:100864
电话: 86 10 68597114(总机) 86 10 68597289(总值班室)














